
Title
FDA發布最終命令,7種類別的手套需提交510(k)


發布時間:2021/7/29 15:35:00 文章來源:百度新聞 點擊量:2700
今年1月15日,衛生與公眾服務部(HHS)發布一則通告,將部分1類和2類產品注冊路徑下調為免于510k注冊,其中豁免的1類產品包含7種類別,全部為手套,如下方截圖所示。
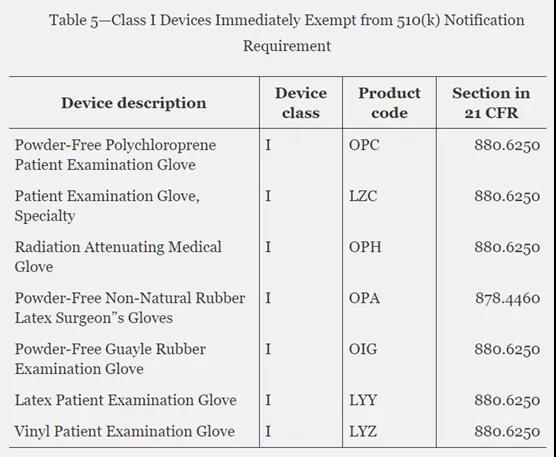
7月26日,HHS和FDA發布最終命令,明確上述7種類別手套,調整為上市前通知(pre-market notification)注冊,不再豁免。強制執行日期為2021年8月25日。意味著在今年1月到7月之間,按照豁免510k路徑注冊的手套產品,需按照最新要求,進行510k申報。
7月26日最終命令的官方鏈接:
HHS和FDA調整注冊路徑的理由是:
這些手套在預防人體健康受損或防止潛在不合理疾病或傷害風險方面具有重大意義,因此,根據FD&C法案第 510(k)節,這些手套必須遵守報告要求。外科醫生手套和病人檢查手套通常是為了防止污染和病原體的傳播,并且可能是防止傳播感染的關鍵屏障。根據4月16日的通知,外科醫生手套可防止手術室受到污染,醫用手套防止例如化療藥物的職業照射,這些手套在保護公眾方面發揮了重要作用。因此,根據第510(k)進行審查是必要的,以便合理保證其安全性和有效性,包括確保手套的耐用和防滲等性能。


